Pylopass™ – Lactobacillus reuteri
Santé gastro-intestinale
Pylopass™ est une souche brevetée de Lactobacillus reuteri qui offre une nouvelle approche dans le contrôle d’Helicobacter pylori : premier facteur de risque des ulcères & gastrites.
Pylopass™ a un mode d’action unique ; Lactobacillus reuteri se coagrège de manière spécifique avec Helicobacter pylori et réduit ainsi sa charge bactérienne dans l’estomac.
Pylopass™ est disponible en France et au Benelux.
Pylopass™ est une souche de Lactobacillus reuteri (DSM 17648) comportant plus de ≥ 1 x1011 cellules inactivées/gramme.
Celui-ci est un ingrédient pour la santé gastro-intestinale qui permet le contrôle d’Helicobacter pylori dans l’estomac.
Pylopass™ a été sélectionné parmi plus de 700 souches sauvages d’espèces de lactobacilles pour sa capacité à agir comme antagoniste de Helicobacter pylori.
1. Mécanisme d'action
Connue par la communauté scientifique, Lactobacillus reuteri est une bactérie lactique appartenant aux bactéries autochtones chez l’homme et l’animal. Cette bactérie est une bactérie à gram positif, non sporulée, en forme de bâtonnet.
Helicobacter pylori est quant à elle une bactérie à gram négatif de forme en spirale qui colonise l’estomac. Aujourd’hui, cette bactérie est la cause majeure des ulcères et des gastrites. On estime que 50% de la population mondiale est infectée par cette bactérie et ce de manière encore plus importante dans les pays en voie de développement avec une prévalence pouvant aller jusqu’à 90 % (Go MF, 2002). Selon Kusters et al. (2006), la sévérité des symptômes est liée à la charge bactérienne et une gastrite non traitée peut entraîner un cancer.
Ainsi, Pylopass™ est une solution très intéressante contre H. pylori grâce à un mode d’action unique.
Lactobacillus reuteri se lie spécifiquement à H. pylori dans l’estomac. Les molécules d’adhésion à la surface du Pylopass™ reconnaissent et adhérent à la surface de Helicobacter pylori. Il y a formation d’agrégats dans l’estomac qui sont ensuite excrétés à travers le tractus digestif et éliminés de l’organisme. (Figure 1)
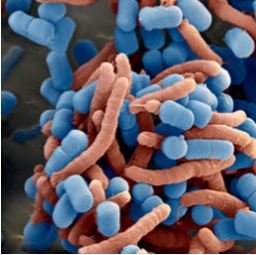
Figure 1 : Co-agrégation du Pylopass™(colorisé en bleu) et de H. pylori (colorisée en rouge)
(Scanning electron microscopy 11 000 x magnification). (Holz C. et al, 2014)
2. Procédé de fabrication
Pylopass™ est obtenu par un procédé de fermentation et un séchage (atomisation) à partir de cellules de Lactobacillus reuteri. Celui-ci est effectué à basse température pour éviter la dénaturation des molécules d’adhésion à la surface des cellules. La fermentation est standardisée et a pour objectif la formation des structures responsables de la co-agrégation sur la membrane afin de garantir une activité maximale.
Les cellules de Lactobacillus reuteri sont inactivées lors du procédé. Cela permet au Pylopass™ d’être stable dans les conditions gastriques. En effet, son mécanisme d’action ne dépend pas de sa survie dans l’estomac et celui-ci ne déséquilibre pas la flore intestinale.
Sources
- Go MF (2002). Review article: Natural history and epidemiology of Helicobacter pylori infection. Aliment Pharmacol Ther 16: 3–15.
- Kusters JG, van Vliet AHM, Kuipers EJ (2006) Pathogenesis of Helicobacter pylori infection. Clin Microbiol Rev 19:449–490.
- Malfertheiner P, Megraud F, O’Morain CA, Atherton J, Axon AT, Bazzoli F, Gensini GF, Gisbert JP, Graham DY, Rokkas T, El-Omar EM, Kuipers EJ, Kuipers EJ (2012) Management of Helicobacter pylori infection—the Maastricht IV/Florence consensus report. Gut 61:646–664 7.
- Wu TS, Hu HM, Kuo FC, Kuo CH (2014) Eradication of Helicobacter pylori infection. Kaohsiung J Med Sci 30:167–172.
- Holz C. et al. (2014). Significant Reduction in Helicobacter pylori Load in Humans with Non-viable Lactobacillus reuteri DSMZ17648: A Pilot Study. Probiotics & Antimicro. Prot.
Différentes études ont été effectuées sur le mécanisme d’action et les bénéfices du Pylopass™ sur la santé.
Pylopass™ permet la réduction de la colonisation de H pylori dans l’estomac, premier facteur de risque des ulcères et gastrites, grâce à son mécanisme d’action unique.
Son rôle est cautionné par six études. Les résultats majeurs de l’étude de Mehling et Busjahn de 2013 et de Holz et al. de 2014 (étude in vitro et pilote) vont être présentés ici.
1. Résultats in vitro
En premier lieu, l’étude in vitro de Holz et al. a permis d’évaluer l’efficacité de Lactobacillus reuteri DSM 17648, souche du Pylopass™.
La co-agrégation de Lactobacillus reuteri DSM 17648 avec la souche de H. pylori DSM 21031 a été observée par microscopie à fluorescence (figure 1 (a)).
Une seconde observation de la co-agrégation de ces mêmes souches a été effectuée dans un milieu reproduisant les conditions gastriques (pH= 4, jus gastrique artificiel, pepsine 0.3%, chlorure de sodium 0.5%) (figure 1 (b)).
Sur la figure 1 (a – B), la co-agrégation des deux bactéries est clairement mise en évidence au microscope. Sur la figure 1 (b), la co-agrégation des deux bactéries est également observable à l’œil nu, il y a en effet un changement visible dans le bécher B tandis qu’aucun changement n’est observé dans les milieux de culture où l’on retrouve soit H. pylori, soit Lactobacillus reuteri (A et C).
Ces premiers résultats in vitro mettent en lumière le mécanisme spécifique du Pylopass™.
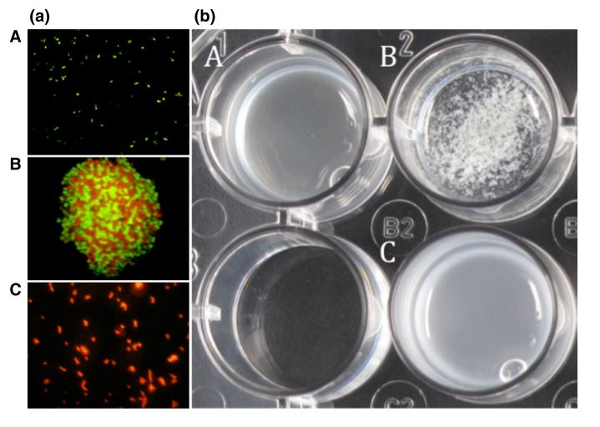
Figure 1 : Analyse microscopique (a) et macroscopique (b) de la coagrégation de Lactobacillus reuteri et d’Helicobacter pylori.
Légende :
(a) (A) H. pylori colorée à l’hexidium iodide
(B) Coagrégation de H. pylori et de Lactobacillus reuteri
(C) Lactobacillus reuteri colorée au carboxyfluorescein diacetate succimidyl ester (CFDA)
(b) (A) H. pylori
(B) Coagrégation de H. pylori et Pylopass™
(C) Pylopass™
2. Résultats de l'étude pilote
Ensuite, l’étude clinique de Mehling et Busjahn publiée en 2013 a évalué l’effet de la supplémentation en Pylopass™ sur Helicobacter Pylori. L’étude est une étude contrôlée, croisée, en simple aveugle sur 22 participants d’âge moyen 47 ans contaminés par H. pylori et asymptomatiques. Les sujets ont reçu un placebo pendant 14 jours puis le Pylopass™, 200 mg/jour pendant 14 jours également. Les 200 mg/jour sont administrés sous forme de quatre comprimés, deux lors du petit déjeuner et deux lors du dîner.
Le test UBT
L’infection bactérienne d’Helicobacter pylori est mesurée par test respiratoire à l’urée marquée au carbone 13 C (Urea Breath Test – UBT). Cette méthode non invasive est fondée sur la capacité d’Helicobacter pylori à synthétiser l’uréase, responsable de l’hydrolyse de l’Urée. (Figure 2). Helicobacter pylori convertit donc l’urée, marquée au carbone 13 C en dioxyde de carbone et en ammonium.
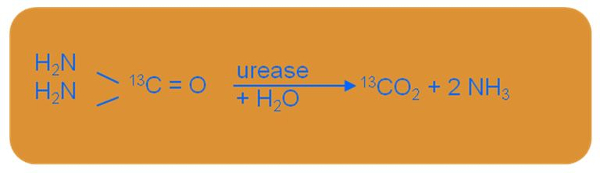
Figure 2: Réaction d’hydrolyse de l’urée causée par Helicobacter pylori (Organobalance, 2016).
Une solution d’urée marquée (75 mg) est ingérée par le sujet puis une certaine quantité de dioxyde de carbone marquée expirée est mesurée. L’échantillon d’air expiré est mesuré avant ingestion (T0) et 30 minutes (T30) après par spectrophotométrie de masse et permet le calcul de la valeur UBT.
Le test est effectué au début de l’étude, après 14 jours de supplémentation avec le placebo et après 14 jours de supplémentation avec le Pylopass™.
Le test est positif si le rapport 13C/12C (12 C : carbone naturel expiré) subit une augmentation de 4‰ après trente minutes (valeur UBT).Cela signifie que l’individu est infecté par Helicobacter pylori.
Labenz et al. (1993) et Zagari et al. (2005) montrent qu’il existe une relation quantitative entre l’activité de l’uréase et la quantité de 13 C chez les sujets à jeûn et ainsi une relation indirecte avec le niveau de colonisation d’H. pylori. Dans l’étude, un niveau de colonisation modérément élevé est défini si la valeur UBT est supérieure à 12‰. Les participants sont sélectionnés au début du test à partir de cette valeur (UBT>12). Un test statistique non paramètrique de Wilcoxon est appliqué pour comparer l’effet du placebo et du Pylopass™.
La figure 3 présente les variations relatives de la valeur UBT après 14 jours de Placebo (en bleu) et après 14 jours de Pylopass™ (en marron) par rapport à la valeur basale.
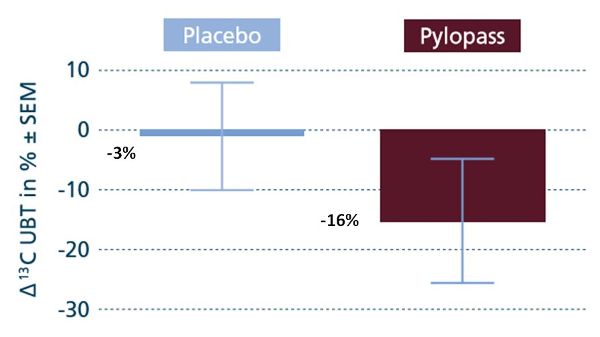
Figure 3: Comparaison du placebo et du Pylopass™.
Il a une diminution significative de – 16% (16 ‰ vs 20‰, p < 0.05) de la valeur du test UBT après 14 jours de supplémentation avec le Pylopass™. La diminution de -3% dans le groupe placebo n’est pas significative.
Holz et al. (2014) ont également étudié l’effet de deux semaines de supplémentation en Pylopass™ sur la charge bactérienne de Helicobacter pylori dans l’estomac. L’étude est une étude pilote contrôlée, croisée, randomisée, en simple aveugle sur 24 participants.
Les participants étaient au départ contaminés par Helicobacter pylori mais n’ont pas encore de symptômes.
Ils ont reçus quatre comprimés à avaler, deux au petit déjeuner et deux au dîner. Chaque comprimé contient 5×109 cellules inactivées de Lactobacillus reuteri lyophilisés (équivalent à 200 mg de Pylopass™).
La charge bactérienne de H. pylori a été mesurée par test UBT au début de l’étude (valeur basale) et après deux semaines.
Après 14 jours de supplémentation avec Pylopass™, il y a une réduction significative de la valeur du test UBT (-4.9 ± 7.8, p = 0.026 vs. placebo) par rapport au groupe placebo (-0.6 ± 5.3) et donc une réduction de la contamination par H. pylori.
- En conclusion, le Pylopass™ permet une réduction significative de la charge bactérienne d’Helicobacter pylori dans l’estomac et donc une diminution des risques d’ulcères et de gastrites.
Pour plus d’informations sur le Pylopass™:
Sources
- Mehling H et al. (2013). Non-Viable Lactobacillus reuteri DSMZ 17648 (Pylopass™) as a New Approach to Helicobacter pylori Control in Humans. Nutrients 5, 3062-3073
- Holz C. et al. (2014). Significant Reduction in Helicobacter pylori Load in Humans with Non-viable Lactobacillus reuteri DSM17648: A Pilot Study. Probiotics & Antimicro. Prot.
La souche du Pylopass™ fait partie de la collection Novozymes Berlin GmbH, anciennent Organobalance.
Pylopass™ a été sélectionnée pour sa qualité d’antagoniste d’Helicobacter pylori.
Statuts
Pylopass™ appartient à la liste des microorganismes ayant obtenu le statut QPS (Présomption d’innocuité reconnue) défini par l’EFSA en Europe (2007) grâce à son utilisation sûre dans l’alimentation.
Elle possède le statut GRAS aux Etats-Unis.
Une souche brevetée
Elle a été déposée à l’Institut Leibniz, banque allemande de microorganismes et cultures cellulaires sous le numéro DSM 17648.
L’utilisation de Lactobacillus reuteri (DSM 17648.) contre Helicobacter pylori est protégée en Europe par le brevet EP1963483 B1.
Un second brevet EP2717890 B1 protège également l’utilisation des souches de Lactobacillus séchées par atomisation contre H. pylori.
Informations complémentaires
Pylopass™ est une souche non allergène (1), non OGM (2), sans gluten (3), halal et adaptée aux végétariens.
Sources
- (1) Annexe II du Réglement (EU) No 1169/2011
- (2) Réglements n°1829/2003/EC, 1830/2003/EC
- (3) Codex Stan 118-197
Le Pylopass™ peut être utilisé dans la formulation de compléments alimentaires ; capsules molles, gélules, comprimés, sachets, etc.
Il peut être aussi utilisé dans les boissons en poudre.
La dose recommandée par jour, définie grâce aux études cliniques, est de 200 mg (2×10^10 cellules). Cette quantité peut être répartie au cours de différentes prises.
1 g de Pylopass™ correspond à environ 100 milliards de cellules de Lactobacillus reuteri.
Le Pylopass™ est un ingrédient très stable qui n’a pas besoin d’être réfrigéré car contrairement aux probiotiques, ces souches inactivées tolèrent parfaitement les changements de conditions environnementales.
Laissez-nous vos coordonnées pour accéder au replay du webinar sur le Pylopass™
Actif's Hors série - Pylopass ™ un probiotique inactivé pour la réduction du risque de gastrites et d'ulcères
Extrait paru dans le hors série Actif’s de 2018 :
« Pylopass™ un probiotique inactivé pour la réduction du risque de gastrites et d’ulcères. »
…
« Pylopass™, probiotique « inactivé » est donc une bonne alternative aux traitements classiques grâce à un mode d’action qui n’entraîne pas de résistances et sans effets secondaires »
Source : Hors série Actif’s de 2018

RIA
RIA Mai 2017 – Extrait :
« Probiotique contre les ulcères…cet ingrédient très stable peut être utilisé dans un grand nombre d’applications finales : compléments alimentaires, capsules molles, gélules, comprimés, sachets et boissons en poudre ».

lesphytonautes.fr
Article paru dans Lesphytonautes.fr :
Les probiotiques contre Helicobacter pylori ?
Extrait : « Lactobacillus reuteri, une souche d’espoir
Mode d’action du probiotique
Des travaux ont été menés dans l’objectif d’évaluer l’effet des probiotiques sur la lutte contre Helicobacter pylori. »
Lire la suite : https://www.lesphytonautes.fr/probiotiques-contre-helicobacter-pylori/